比較表1���、2可以看出,Na+����、K+�、NH+4�����、Mg2+���、Ca2+對中性蛋白酶的激活作用比堿性蛋白酶激活作用更大����,即有利于中性蛋白酶的催化作用。這是由于許多酶促反應必須有其他適當物質(zhì)存在時才能表現(xiàn)酶的催化活性或加強其催化效力�。一般認為,金屬離子的激活作用是由于金屬離子與酶結合��,此結合物又與底物結合成三位一體的“酶—金屬—底物”的復合物,這里金屬離子使底物更有利于同酶的活性(部位)的催化部位和結合部位相結合使反應加速進行���。金屬離子在其中起到了某種搭橋的作用�。當濃度過大時,由于溶液的離子化效應使酶的活性反而降低���。氧化性強的物質(zhì)或重金屬的存在,可能是因為酶是蛋白質(zhì),而這些鹽使蛋白質(zhì)變性,從而使酶變性而失活�,不利于酶的催化水解�����。
3.2蛋白酶與表面活性劑的關系
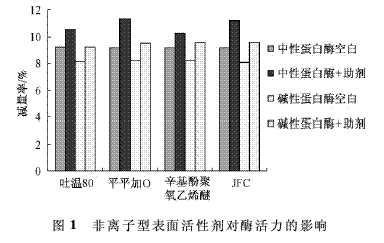
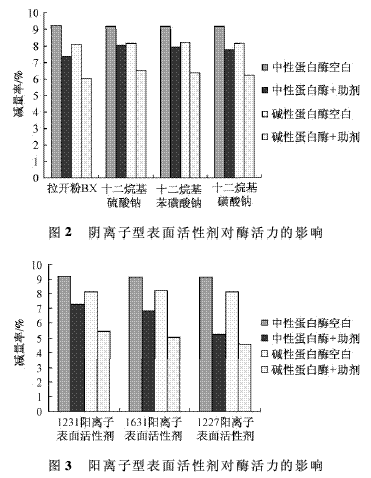
表面活性劑具有潤濕�、滲透��、乳化和分散等功能���,由于蛋白酶通常與表面活性劑混用�,因此有必要對不同離子類型的表面活性劑對酶活性的影響進行研究��。本文實驗����,在相同的實驗條件下,通過測定減量率來研究不同離子型表面活性劑對蛋白酶M的作用效果�。不同類型表面活性劑對酶活力的影響結果見圖1~3。

 您所在的位置:
您所在的位置:












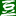



編.gif)